[ソウル/ヘルスコリアニュース] 食品医薬品安全処は4日、㈱セルリード(CELLID Co., Ltd.)の「AdCLD-CoV19」と震源生命科学㈱(GeneOne Life Science Co., Ltd.)の「GLS-5310」など国内開発コロナ19ワクチン2種に対する臨床試験をそれぞれ承認した。 これを受け、国内で食薬処の承認を受けた「コロナ19」ワクチンの臨床試験は合わせて5件に増えた。
(セルリードのコロナ19ワクチン「AdCLD-CoV19」臨床試験について)
今回の臨床試験は、健康成人を対象にワクチンの安全性及び免疫原性を評価するための12相臨床試験である。 免疫原性とは、ウイルス感染性を取り除いたり低下させたりする「中和抗体」の増加率をいう。
該当ワクチンはコロナ19ウイルスの「表面抗原遺伝子」をアデノウイルス鋳型に入れて製造した「ウイルスベクターワクチン」だ。
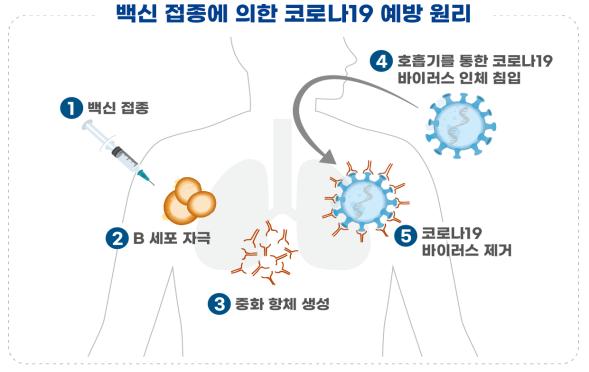
予防原理はアデノウイルス鋳型を通じてヒト細胞内に伝達された表面抗原遺伝子が体内で表面抗原タンパク質を合成して中和抗体生成を誘導し、以後コロナ19ウィルスが侵入した時、この中和抗体がコロナ19ウィルスを除去することだ。
ちなみに、国外でもウイルスベクタープラットフォームのコロナ19ワクチンに対する三相臨床試験が進められている。 英国のアストラゼネカ社、中国のカンシノ社、ロシアのガマレヤ研究所、米ジョンソン·アンド·ジョンソン社などがこのようなワクチンを開発している企業だ。
(震源生命科学のコロナ19ワクチン「GLS-5310」臨床試験について)
このワクチンも健康な成人を対象に当該ワクチンの安全性及び免疫原性を評価するための12相臨床試験だ。
該当ワクチンはコロナ19ウイルスの「表面抗原遺伝子」をDNA(プラスミド)の形で製造した「DNAワクチン」だ。
予防原理は接種したコロナ19ウィルス表面抗原遺伝子によって体内で表面抗原タンパク質を合成して中和抗体生成を誘導し、以後コロナ19ウィルスが侵入した時、この中和抗体がコロナ19ウィルスを除去することだ。
ちなみに、国内外でDNAワクチンプラットフォームのコロナ19ワクチンに対する臨床試験が進められている。 (国内企業としては、ジェネクシン社の2相臨床試験、米国イノビオ社の2相臨床試験がある。
食薬処が先に臨床試験を承認した3件のコロナ19 ワクチンは、コロナ19 ウイルスの表面抗原遺伝子(DNA)を注入し、体内で表面抗原タンパク質を生成することで免疫反応を誘導するDNA ワクチンか、遺伝子組み換え技術を利用して製造したコロナ19 ウイルスの「表面抗原タンパク質」を体内に直接注入して免疫反応を誘導する組換えワクチンである。
(ヘルスコリアニュース / http://www.hkn24.com)






